| 结构式 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| K | |||||||||
| 常规 | |||||||||
| 名字 | 亚硝酸钾 | ||||||||
| 其他名称 | 亚硝酸钾,E 249 | ||||||||
| 分子式 | KNO2 | ||||||||
| CAS号 | 7758-09-0 | ||||||||
| 简短说明 | 白色黄色固体 | ||||||||
| 属性 | |||||||||
| 摩尔质量 | 85.10 克摩尔 | ||||||||
| 物质状态 | 固定 | ||||||||
| 密度 | 1.92 克厘米 | ||||||||
| 熔点 | 441°C | ||||||||
| 沸点 | 分解 | ||||||||
| 溶解度 | 在水中良好(2810 g/L at 20 °C) | ||||||||
| 安全说明 | |||||||||
| |||||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||||
亚硝酸钾 , 硝酸钾2 (又名:硝酸钾 , 英文:亚硝酸钾 ),是亚硝酸HNO2的钾盐 .
属性
亚硝酸钾形成无色至微黄色、高度吸湿(=吸湿)的晶体,冷却时易溶于水,溶液呈碱性反应。晶体从 360 °C 开始分解。否则,它的行为与亚硝酸钠相似,即它会氧化(特别是在较高温度下)并与金属如铝(特别是粉末形式!)、干燥的铵化合物(如硫酸铵)、氰化物和许多金属发生剧烈反应有机化合物。它是一种还原剂,在空气中缓慢转化为硝酸钾KNO3 氧化了。
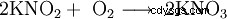
亚硝酸钾有毒;一般来说,亚硝酸盐在合适的条件下会与某些胺类反应生成致癌的亚硝胺。亚硝酸盐可用硫酸亚铁和浓硫酸检测,呈棕色。
发生与产生
在自然界中,亚硝酸盐是氮循环的中间阶段——硝化作用(氮结合)和反硝化作用(氮释放)。从技术上讲,亚硝酸钾是通过氮氧化物对氢氧化钾溶液的作用获得的。
用法
亚硝酸钾可用作编号 E 249 的食品添加剂 (防腐剂)在一定条件下可使用亚硝酸盐固化盐(氯化钠与亚硝酸钾和亚硝酸钠)。它通过形成亚硝基肌红蛋白使肉呈永久红色。肉类和香肠制品的亚硝酸盐含量可能是饮用水限值的倍数。
来源
- ↑ CAS 编号条目。 BGIA 的 GESTIS 物质数据库中的 7758-09-0,于 2007 年 12 月 14 日检索 (需要 JavaScript)



