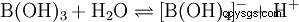| 结构式 | |||||||
|---|---|---|---|---|---|---|---|
| 常规 | |||||||
| 名字 | 硼酸 | ||||||
| 其他名称 | 硼砂 | ||||||
| 分子式 | H3 BO3 | ||||||
| CAS号 | 10043-35-3 | ||||||
| 简短说明 | 白色粉末 | ||||||
| 属性 | |||||||
| 摩尔质量 | 61.83 克/摩尔 | ||||||
| 物质状态 | 固定 | ||||||
| 密度 | 1.44 克/厘米 | ||||||
| 熔点 | 在 185 °C 时分解 | ||||||
| 沸点 | 不存在 | ||||||
| 蒸气压 | 2.7 hPa (20 °C) | ||||||
| 溶解度 | 50克/升在水中 | ||||||
| 安全说明 | |||||||
| |||||||
| MAK | 没有 | ||||||
| LD50 | 2660毫克/公斤 | ||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||
硼酸 (又作:原硼酸 ), H3 BO3 , 是硼的最简单的含氧酸,其盐类称为硼酸盐。 (以前也叫氢氧化硼)
属性
纯硼酸形成鳞片状、无色、有光泽的晶体,熔点为 171 °C。它最初难以溶于水,但随着浓度的增加,这一过程会加速。溶液呈弱酸性反应。与甲醇形成挥发性硼酸甲酯 - 即使没有浓硫酸 - 燃烧时会发出绿色火焰,用于定性硼检测。
当原硼酸被加热时,水被分解并形成偏硼酸HBO2,它发生在几个变体中 最后,进一步除去水,生成三氧化二硼B2 O3 .
尽管有三个氢原子,但硼酸在水中会像一元酸一样发生反应,产生四羟基硼酸根离子 B(OH)4 .这里它不像作为质子供体的布朗斯台德酸,而是像作为氢氧化物受体的路易斯酸:
硼酸是一种非常弱的酸(pK
该反应用于硼酸的碱滴定,也用于凯氏定氮,少量无毒。但是硼烷的毒性很大。
出现与提取
游离硼酸存在于意大利中部托斯卡纳的蒸汽源(喷气孔)中,可以通过在闪亮的薄片中蒸发从这些源中获得酸。硼酸也以矿物萨索林的形式出现在托斯卡纳。然而,碱金属和碱土金属盐,例如矿物孔雀石 Na2,是非常重要的。 B4 O7 · 4H2 O. 一种类似的稀有矿物是硼砂,它含有 8 或 10 当量的结晶水。然而,如今,这主要是从 kernit 获得的。用盐酸或硫酸处理硼砂,得到硼酸B(OH)3 释放。
用法
水溶液(“乏味水”)用作温和的消毒剂,也被批准为防腐剂 E284。硼酸是用于制造硼硅酸盐玻璃、瓷器、搪瓷的中间体,也存在于阻燃剂和媒染剂中。世界硼酸年产量200多吨。
硼酸的另一个应用是在带有压水反应堆的核电站中。在那里,硼酸是因为同位素 B-10 对热中子的吸收系数高,天然硼中的含量为 20%,因此可以控制倍增因子 k,从而控制反应堆的功率。
此外,硼酸用于计算CO2 -古代地球上使用的薪水。在酸性环境中,更多的硼被结合到硼酸中。当 pH 值变为碱性时,硼酸转化为硼酸盐,即硼酸盐。由于有孔虫(化石以及最近的单细胞生物)需要硼酸盐来构建它们的外壳,因此该关系可用于确定地球历史上某个时间点该区域存在的 pH 值。由于这种原生动物的壳以及贻贝等构成了海洋沉积物的主要部分,因此可以简单地从那里取出沉积物核心并在实验室中检查两种硼同位素。这样的结果与被困在冰芯中的气泡有很好的相关性。
硼酸与甲醇结合产生绿色火焰颜色;与其他烷醇有关的绿色火焰边界。此属性在火焰表演中被大量使用,例如为火焰棒、pois 或火碗着色。
来源
- ↑ 材料安全数据表 (Merck)