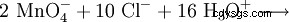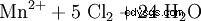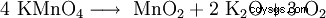| 结构式 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 常规 | |||||||||
| 名字 | 高锰酸钾 | ||||||||
| 其他名称 | 四氧锰酸钾(VII)、锰酸钾(VII)、高锰酸钾(um) | ||||||||
| 分子式 | KMnO4 | ||||||||
| CAS号 | 7722-64-7 | ||||||||
| 简短说明 | 带有金属光泽的深紫色晶体 | ||||||||
| 属性 | |||||||||
| 摩尔质量 | 158.03 克摩尔 | ||||||||
| 物质状态 | 固定 | ||||||||
| 密度 | 2.70g cm | ||||||||
| 熔点 | 240°C以上分解 | ||||||||
| 沸点 | 不适用 | ||||||||
| 蒸气压 | 0.01 mbar(20°C) | ||||||||
| 溶解度 | 在水中适中(20 °C 时为 64 g/L) | ||||||||
| 安全说明 | |||||||||
| |||||||||
| MAK | 0.5 毫克米 | ||||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||||
高锰酸钾 (KMnO4 ) 是高锰酸钾盐,HMnO4,游离态未知 .它是一种深红紫色金属光泽的结晶固体,是一种强氧化剂。高锰酸根阴离子是盐的强烈颜色的唯一原因。这是由于电荷转移复合物的形成。在高锰酸盐中,锰处于最高氧化态,VII。
属性
高锰酸钾形成深红紫色有光泽的晶体,可适度溶于水,即使在低浓度下也会产生强烈的紫色溶液。加热时,晶体不会熔化,而是会随着明显的噼啪声分解,释放氧气。结晶高锰酸钾在室温下稳定,但其水溶液随时间降解。
由于锰以最高氧化态存在于高锰酸根阴离子中,因此在氧化还原反应中它是一种非常强的氧化剂。例如高锰酸钾将盐酸氧化成氯气(实验室制取氯气的方法):
此外,它还可以将亚硫酸盐氧化为硫酸盐,将 Fe(II) 氧化为 Fe(III) 离子,将醇氧化为羧酸。它还可以引起[[有机化学]物质的分解。高锰酸钾具有氧化性。
高锰酸钾在 240 ℃分解成二氧化锰(MnO2 )、氧化钾(K
作为与冠醚的络合物,高锰酸钾还可以在苯、甲苯等非极性有机溶剂中制备,在有机合成化学中得到了开发利用。
制造
技术生产从二氧化锰MnO2开始 与氢氧化钾和大气中的氧气形成绿色锰酸钾(VI)K
用法
由于其强氧化作用,高锰酸钾被用作消毒剂、除臭剂和杀藻剂等。在定量化学分析(氧化测定法、锰测定法、氧化还原滴定法)中,它用于测定大量物质(例如铁、亚硝酸盐、草酸盐以及间接钙);此处测定的终点以紫色表示。在实验室中,也使用碱性高锰酸钾溶液来清洗玻璃器皿。在摄影中,它用于检测定影盐(硫代硫酸钠)并减少过度曝光的图像;这会氧化银。
当甘油滴在过量的盐上时,混合物会在几秒到几分钟后点燃,并以特有的紫色火焰燃烧。由于高温,这种延迟反应被用来启动铝热反应。
医学
在医学上,高锰酸钾溶液用作皮肤外用的收敛剂和消毒剂,例如:用于脚癣或尿布疹(ATC 代码 D08AX06)。在紧急毒理学中,酒红色 高锰酸钾溶液(约 0.1%)用于在摄入可氧化毒素后中毒时进行洗胃。
历史
过去的摄影师使用高锰酸钾作为闪光粉的成分。高锰酸钾用于漱口喉咙痛,在烹饪中用于除臭肉类,使其可以再次食用。
安全说明
高锰酸钾具有 3 级水危害(对水高度危险),除了其氧化作用外,在处理高锰酸盐残留物时必须考虑到这一点。高锰酸钾急性毒性低(LD50 (大鼠,口服) =750 mg/kg),但由于其强氧化作用,对活组织有明显的刺激作用,容易发生化学灼伤。因此,必须防止任何非医疗用途或什至经口摄入以外的接触!高锰酸盐粉尘会导致角膜混浊。
然而,在接触时发生的皮肤本身的变色是无害的,是由高锰酸盐还原过程中形成的二氧化锰引起的。较大的变色区域可以用亚硫酸盐溶液再次漂白。
由于其强氧化作用,高锰酸钾与许多还原性或可燃性物质发生剧烈反应,可发生自燃。与这些不会导致自发反应的物质的混合物极易燃烧,并可能发生爆炸性反应。
<表>来源
- ↑ CAS 编号条目。 BGIA 的 GESTIS 物质数据库中的 6487-48-5,于 2007 年 12 月 15 日检索 (需要 JavaScript)
- ↑ Roth、Daunderer、Kormann:有毒植物 - 植物毒素,ecomed Landsberg,1988,ISBN 3-609-64810-4 , p. 810ff