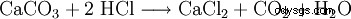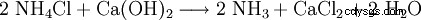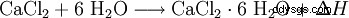| 结构式 | |||||||
|---|---|---|---|---|---|---|---|
| 没有可用的结构式 | |||||||
| 常规 | |||||||
| 名字 | 氯化钙 | ||||||
| 其他名称 |
| ||||||
| 分子式 | 氯化钙2 | ||||||
| CAS号 | 10043-52-4(无水) 10035-04-8(二水合物) 25094-02-4(四水合物) 07774-34-7(六水合物) | ||||||
| 简短说明 | 无色无味的吸湿性晶体 | ||||||
| 属性 | |||||||
| 摩尔质量 | 110.98 g mol(无水) 147.02 g mol(二水合物) 182.04 g mol(四水合物) 219.08 g mol(六水合物) | ||||||
| 物质状态 | 固定 | ||||||
| 密度 | 2.16 g cm(无水) 1.85 g cm(二水合物) 1.71 g cm(六水合物) | ||||||
| 熔点 | 782 °C(无水) 约约 176 °C(二水合物) 35°C(四水合物) | ||||||
| 沸点 | 1935 °C | ||||||
| 蒸气压 | 11 hPa | ||||||
| 溶解度 |
易溶于水:740 g l (20 °C) | ||||||
| 安全说明 | |||||||
| |||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||
|晶体结构||金红石(扭曲),八面体氯化钙 (还有氯化钙 )是碱土金属钙的氯化物,分子式为CaCl2 .钙的氧化态为+2,氯的氧化态为-1。
历史
1860年前后,化学家罗伯特·威廉·本生(Robert Wilhelm Bunsen)和马蒂森(Matthiessen)通过氯化钙的电解,成功地首次纯制了元素钙。
出现次数
氯化钙在自然界中溶解在盐水中。
获取与显示
氯化钙是由盐酸和碳酸钙制成的:
随后加热至 260 °C 提供无水形式。
从技术上讲,氯化钙是通过索尔维工艺生产苏打时作为废品获得的,即从生产的氯化铵中回收氨:
属性
氯化钙是一种盐。由于电负性差异很大,钙和氯以离子形式存在。因此,这种结合是通过静电相互作用发生的。
在其纯净形式中,氯化钙形成无色晶体,并且在无水时具有高度吸湿性。它很容易从周围吸收水分,形成水合物复合物。
反应
氯化钙与水反应形成六水合物并放出大量热量(放热,ΔH> 0):
六水合物的晶体在 30 °C 左右溶解在其自身的结晶水中。通过加热到 200 °C 左右再次释放结合水。与无水氯化钙相比,溶解在水中会导致强烈的冷却。这两种形式的氯化钙也很容易溶于乙醇。
用法
由于其吸湿性,无水氯化钙是实验室中重要的干燥剂,例如在干燥器中,以及用于各种气体和液体的技术化学中。应用领域是生活空间的干燥,用作防冻剂,特别是用作混凝土中的防冻剂和促凝剂,以及用作灰尘粘合剂(例如在建筑工地)。医学上用于止血、治疗缺钙疾病,以及治疗冻疮和过敏。
用作固化剂、增味剂和稳定剂(例如用于饮用水处理、水果表面处理)。在欧盟,它作为食品添加剂编号为 E 509 批准。
氯化钙用于通过与水反应放热水合来加热即饮饮料。它还用作路盐和用于生产冷却混合物(见上文 )。
它还用于食品技术中凝结蛋白质,并用于制造豆腐或人造鱼子酱等产品。
来源
- ↑ BGIA GESTIS 物质数据库:https://www.hvbg.de/d/bia/gestis/stoffdb/index.html . 5 月 9 日。 2007