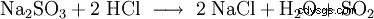| 结构式 | |||||||
|---|---|---|---|---|---|---|---|
| 常规 | |||||||
| 名字 | 二氧化硫 | ||||||
| 其他名称 | 四氧化硫、亚硫酸酐 | ||||||
| 分子式 | SO2 | ||||||
| CAS号 | 7446-09-5 | ||||||
| 简短说明 | 无色,有刺激性,有毒气体 | ||||||
| 属性 | |||||||
| 摩尔质量 | 64.06 克摩尔 | ||||||
| 物质状态 | 气态 | ||||||
| 密度 | 2.73 kg m (1 bar, 15°C) | ||||||
| 熔点 | -75 °C | ||||||
| 沸点 | -10 °C | ||||||
| 蒸气压 | 3.3 巴 (21°C) | ||||||
| 溶解度 | 水中好(112克/升) | ||||||
| 安全说明 | |||||||
| |||||||
| MAK | 1.3 毫克 m | ||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||
二氧化硫 , 所以2 , 是亚硫酸 H2 的酸酐 所以3 .二氧化硫是一种无色有毒气体,有刺激性气味和酸味。它主要在燃烧含硫量高达 4% 的煤或石油产品等含硫化石燃料时产生。因此,它对空气污染的贡献很大,它是酸雨的原因,二氧化硫首先被氧气氧化形成三氧化硫,然后与水形成硫酸(H2 所以4 )实施。为了防止这种情况,烟气脱硫有多种工艺。
制造
- 通过燃烧硫磺或硫化氢
- 通过焙烧硫化矿石
例如B.黄铁矿:
-

- 二硫化铁 (II) 和氧气反应生成氧化铁 (III) 和二氧化硫。
- 通过强酸从亚硫酸盐中提取
属性
| E号 | 220 |
| 临界温度 | 157.5°C |
| 临界压力 | 7.9 巴 |
二氧化硫的介观极限公式如下:
笼统地说:
液态二氧化硫可溶解多种物质,因此已成为一种有价值的溶剂。
用法
二氧化硫在食品工业中的名称为 E 220 用作防腐剂和抗氧化剂,特别适用于干果、马铃薯菜肴、果汁、果酱和葡萄酒。也用于生产硫酰氯SO2 氯2 和亚硫酰氯 SOCl2 .
此外,二氧化硫是生产三氧化硫的重要原料,用于生产浓硫酸,例如硫酸。 B.用联系方式。
二氧化硫还用于制造许多化学品、药物和染料,以及用于漂白纸张和纺织品。
污染
在高浓度时,二氧化硫会损害人类、动物和植物。氧化产物导致“酸雨”,危及森林和湖泊等敏感生态系统,并侵蚀建筑物和材料。
在过去的二十年里,发达国家通过使用低硫或无硫可燃物和燃料,大大减少了 SO2 总排放量。
安全说明
高于 MAK 值的二氧化硫浓度会导致人类头痛、恶心和嗜睡。在较高浓度下,气体会严重损害支气管和肺,甚至会损害遗传特性的载体核酸。
来源
- ↑ 材料安全数据表(普莱克斯)
- ↑ BGIA Gestis 有害物质数据库
- ↑ Holleman-Wiberg:无机化学教科书 第 102 版,de Gruyter,柏林,2007 年。