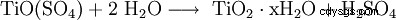| 结构式 | |||||||
|---|---|---|---|---|---|---|---|
| 没有可用的结构式 | |||||||
| 常规 | |||||||
| 名字 | 氧化钛(IV) | ||||||
| 其他名称 |
| ||||||
| 分子式 | O2 钛 | ||||||
| CAS号 | 13463-67-7 | ||||||
| 简短说明 | 白色结晶性粉末 | ||||||
| 属性 | |||||||
| 摩尔质量 | 79.90 克摩尔 | ||||||
| 物质状态 | 固定 | ||||||
| 密度 | 4.24 克厘米 | ||||||
| 熔点 | 1855°C | ||||||
| 沸点 | 2900°C | ||||||
| 溶解度 | 不溶于氢氟酸、浓硝酸和硫酸,不溶于水、盐酸、稀硝酸和硫酸 | ||||||
| 安全说明 | |||||||
| |||||||
| 热力学性质 | |||||||
| ΔHf | −249 kJ/mol(金红石) | ||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||
氧化钛(IV) (二氧化钛 ) 是钛的氧化物之一。
出现次数
氧化钛(IV)以三种形式自然生成:
- 金红石是一种四方矿物,主要呈棱柱状。 金红石这个名字 来自拉丁语rutilus – 微红。金红石的密度为 4.26 g/cm。它作为一种白色颜料特别受欢迎。
- 锐钛矿形成四方全面体晶体(全面体是指晶体系统中最对称的基团,在四方体中因此为 4/m 2/m 2/m)。锐钛矿逐渐(从超过 700 °C 的温度开始更快)不可逆地转变为金红石。锐钛矿的密度为 3.88 g/cm。锐钛矿也可用作白色颜料。
- Brookite 形成正交矿物,不用作白色颜料。 Brookite 在熔点以下也会变成金红石。
由于天然沉积物具有令人不安的颜色,因此 z。 B.由钛铁矿中的铁(FeTiO3 ) 造成的,这些在硫酸盐工艺或氯化物工艺中进行精制(首选)。
获取与显示
通过Ti(IV)化合物的溶剂分解(水解):
属性
二氧化钛的熔点为1855℃。它具有热稳定性、耐用性、高折射率 (2.8),因此具有出色的着色和遮盖力。二氧化钛在化学上是非常惰性的。它耐光、价格低廉、完全无毒,因此是最重要的白色颜料。
用法
二氧化钛用作白色着色剂。它于 1908 年在挪威和美国被发现,并于 1909 年以 Kronos Titanium White 的名称在那里制造。 1924 年在德国开始生产,名称为 Degea-Titanweiß。直到 1938 年,钛白才以锐钛矿形式生产,但后来主要以金红石形式生产,证明对油粘合剂和有机染料更稳定。因此也被称为金红石白。
钛白在所有白色颜料中具有最高的不透明度和出色的增亮能力。它具有化学稳定性、无毒的特性,可以在名称 E 171 下找到,例如作为牙膏和止咳药水的食品添加剂。它有时也用于油画。在技术领域,它用于油漆和清漆(例如用于墙壁油漆和纺织品)、纸张以及作为防晒霜中的紫外线阻断剂和药物(片剂)中的增白剂。 TiO2的光催化作用 纳米粒子用于“自清洁”表面(光催化自清洁)的紫外线活性。染料太阳能电池(Grätzel 电池)再次基于二氧化钛的半导体特性。二氧化钛还用作一级陶瓷电容器中陶瓷介质的主要成分。
锐钛型二氧化钛是SCR工艺烟气工业脱硝催化剂的主要成分。
使用硫酸法生产二氧化钛会产生稀酸(稀硫酸),其中一部分通过浓缩再用于生产二氧化钛。在一些国家,部分稀酸仍排入河流和海洋或倾倒,而氯化法则不产生任何稀酸。所用的氯主要留在工艺循环中。
二氧化钛2 也用于瓷砖修整领域,这意味着处理过的瓷砖表面具有防污性。
证明
在寒冷中新沉淀的二氧化钛是两性的,可溶于稀无机酸。在瓷坩埚中用硫酸氢钾进行消解。然后用少量硫酸将其溶解在冷水中。用几滴过氧化氢,将黄色(碱性)变为橙黄色(酸性,照片)[Ti(O2 ) aq] 阳离子。盐酸和锌(颗粒)形成初生氢,将 Ti(IV) 转化为红紫色 [Ti(H2 O)6 ] 减少。
纳米技术
个人证明
- ↑ BGIA 的 GESTIS 物质数据库中关于氧化钛 (IV) 的条目,检索于 2007 年 11 月 29 日 (需要 JavaScript)
- ↑ Susanne Donner:用光的力量清洁 .技术评论,第 7 期,2006 年 7 月,第 19 页。