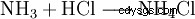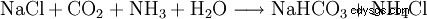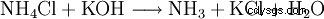| Strukturformel | ||||||||
|---|---|---|---|---|---|---|---|---|
| Allgemeines | ||||||||
| 名字 | 氯化铵 | |||||||
| 安德烈·纳曼 |
| |||||||
| 总结形式 | NH4 氯 | |||||||
| CAS 编号 | 12125-02-9 | |||||||
| 库兹贝施雷布恩 | 魏斯·克里斯塔尔 | |||||||
| Eigenschaften | ||||||||
| 摩尔质量 | 53,49 g·mol | |||||||
| 集合体 | 节日 | |||||||
| 说辞 | 1,526 克·厘米 | |||||||
| Schmelzpunkt | 335 °C | |||||||
| 西德朋克 | 关闭 | |||||||
| 湿疹 | 1,3 hPa (160,4 °C) | |||||||
| 失恋 | Wasser 肠道 (372 g/L 20°C) | |||||||
| 安全感 | ||||||||
| ||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet。 Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen。 | ||||||||
氯化铵 (NH4 Cl) ist ein weißes, gut wasserlösliches Salz, welches kubische Kristalle bildet。
Mit steigender Temperatur dissoziiert Ammoniumchlorid zunehmend zu Ammoniak und Chlorwasserstoff。北 340 °C sublimiert der Stoff volllständig。 Unter Druck (34,4 bar) schmilzt Ammoniumchlorid bei 520 °C.Als Lebensmittelzusatz trägt es die Nummer E 510。
前锋
Natürlich vorkommendes Ammoniumchlorid ist als Mineral Salmiak bekannt und 动词。 Der Name "Salmiak" leitet sich von lat。 "sal ammoncum " (Salz des Ammon, siehe auch Namensherkunft von Ammoniak) ab, da es im Altertum in der Nähe eines Ammon-Tempels im heutigen Ägypten vorkam und mit Halit (Steinsalz) verwechselt wurde。
Gewinnung 和 Darstellung
Ammoniumchlorid kann durch Neutralization von wässriger Ammoniaklösung mit Salzsäure oder durch die Reaktion von gasförmigem Ammoniak mit gasförmigen Chlorwasserstoff gewonnen werden。 Es kann durch Umkristallisieren aus Wasser gereinigt werden。
Ammoniumchlorid fällt als Nebenprodukt bei der Gewinnung von Soda nach dem Solvay-Verfahren an.
特征结构
Wasser löslich 的氯化铵肠胃。 Wässrige Lösungen reagieren sauer。 Der pH-Wert einer 1%igen Lösung beträgt etwa 5,5。 Ethanol löslich 中的 Esist schlecht 和 Aceton 和 Ether 中的 unlöslich。
Beim Versetzen von Ammoniumchlorid mit starken Basen wird gasförmiges Ammoniak freigesetzt。
验证
Verwendung findet Ammoniumchlorid heute unter anderem zur Herstellung von Kältemischungen,在 der Färberei und Gerberei。 Ebenfalls findet es Anwendung beim Verzinnen, Verzinken oder Löten, da es die Fähigkeit besitzt, mit Metalloxiden flüchtige Chloride zu bilden und somit die Metalloberfläche zu reinigen。 Des Weiteren dient es in der Medizin als Expektorans und wird als Elektrolyt in Zink-Kohle-Batterien eingesetzt; Salmiak-Lakritz 的 außerdem。 Es ist auch häufig 在 Rauchpulver (weiß) vorhanden。
奎伦
- ↑ BGIA GESTIS Stoffdatenbank:https://www.hvbg.de/d/bia/gestis/stoffdb/index.html . 2007 年 8 月 15 日
文学
- Pradyot Patnaik:无机化学品手册 .麦格劳希尔,纽约 2002 ISBN 0-07-049439-8 (英语)