| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
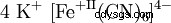 | |||||||
| Allgemeines | |||||||
| 名字 | 六氰化钾(II) | ||||||
| 安德烈·纳曼 |
| ||||||
| 总结形式 | C6 FeK | ||||||
| CAS 编号 |
| ||||||
| 库兹贝施雷布恩 | zitronengelbe Kristalle | ||||||
| Eigenschaften | |||||||
| 摩尔质量 | 368,34 g·mol (wasserfrei) | ||||||
| 集合体 | 节日 | ||||||
| 说辞 | 1,85 g/cm (wasserfrei) | ||||||
| Schmelzpunkt | 北加州。 70 °C Kristallwasserabgabe des Trihydrats | ||||||
| 西德朋克 | > 400 °C (Zersetzung) | ||||||
| 失恋 | Wasser 中的肠道 löslich:337 g/l (20 °C) | ||||||
| 安全感 | |||||||
| |||||||
| 马克 | 不为所动 | ||||||
| WGK | 2 | ||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet。 Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen。 | |||||||
六氰化铁钾(II) ist ein Salz mit der Konstitutionsformel K
Herstellung
Hergestellt wird Kaliumhexacyanidoferrat(II) aus einer Eisen(II)-Salzlösung und Kaliumcyanid。 Es enthält dann Kristallwasser und liegt als K
Unter Normalbedingungen ist das Hexacyanidoferrat(II)-Ion jedoch ein stabiler Komplex, esist daher ungiftig。
Früher wurde Kaliumhexacyanidoferrat(II) durch Glühen von eingetrocknetem Blut, Hornspänen und anderen tierischen Substanzen mit Eisenspänen und Pottasche hergestellt, daher auch die Bezeichnung als Gelbes Blutlaugensalz。
验证
In der Analytik wird das Salz zum Nachweis von Eisen(III)-Ionen verwendet。 In Lösung erhält man bei Zugabe von Fe-Ionen zunächst lösliches Berliner Blau, K[FeFe(CN)6 ], durch einen Überschuss fällt unlösliches Berliner Blau aus, Fe[FeFe[(CN)6 ]3 . Diese Reaktionen dienen zum Nachweis von Eisen(III)-Ionen:
Aus Kaliumhexacyanidoferrat(II) lässt sich durch Oxidation mit Wasserstoffperoxid Kaliumhexacyanidoferrat(III) herstellen。
在 der Lebensmittelindustrie wird Kaliumhexacyanidoferrat als Trennmittel und Stabilisator verwendet。 Es darf in Lebensmitteln jedoch nur in geringen Mengen verwendet werden, da sich beim Erhitzen oder bei Einwirkung von Säuren Blausäure bilden kann.Es ist in der EU als Lebensmittelzusatzstoff der Bezeichnung E536 ausschließlich für die Verwendung in Kochsalz und Kochsalzersatz zugelassen。
奎伦
- ↑ Eintrag zu Kaliumhexacyanidoferrat(II) in der GESTIS-Stoffdatenbank des BGIA,abgerufen am 31.8.2007 (JavaScript erforderlich)
- Kaliumhexacyanidoferrat (III) (rotes Blutlaugensalz)
- 氰化物

