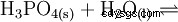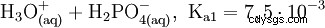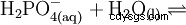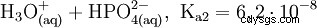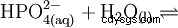| 结构式 | |||||||
|---|---|---|---|---|---|---|---|
| 常规 | |||||||
| 名字 | 磷酸 | ||||||
| 其他名称 | 正磷酸 | ||||||
| 分子式 | H3 采购订单4 | ||||||
| CAS号 | 7664-38-2 | ||||||
| 简短说明 | 无色无味固体 | ||||||
| 属性 | |||||||
| 摩尔质量 | 98.00 克摩尔 | ||||||
| 物质状态 | 固体(通常是液体,因为过冷的熔体可以储存很长时间) | ||||||
| 密度 | 1.834g cm (18°C) | ||||||
| 熔点 | 42.35°C | ||||||
| 沸点 | 分解:213°C(脱水) | ||||||
| 蒸气压 | 3.8帕(20℃) | ||||||
| pKa值 | 2.16; 7.21; 12.32 | ||||||
| 溶解度 | 与水完全混溶,易溶于醇 | ||||||
| 安全说明 | |||||||
| |||||||
| MAK | 2 mg m(可吸入气溶胶部分) | ||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||
正常 或邻- 磷酸 是磷的主要酸。无水物质是高度吸湿的。它是一种三元酸,相对于第一次去质子化反应为中等强酸。缩合物二磷酸、偏磷酸和多磷酸均由其衍生。作为食品添加剂,磷酸被列为E 338 声明。
获取与显示
磷酸可由磷酸岩(多为磷灰石、Ca5 (PO4 )3 (F, OH, Cl)) 与硫酸、盐酸或硝酸。 CaSO4 作为副产物形成 (硬石膏、石膏)和H2 [SiF6 ](六氟硅酸)。或者,磷酸可以通过燃烧元素磷形成五氧化二磷,P4来获得 O10 ,以及随后的水解(所谓的热磷酸)。
属性
磷酸是一种三元酸,可以在三个阶段以溶剂化质子的形式提供其氢,形成磷酸二氢根、磷酸氢根和磷酸根阴离子。相关的pKs值为pK
用法
磷酸用作生产含磷酸盐肥料(美国产量的 90% 以上)、清洁剂、除锈剂或除锈剂的原料,以及用于钝化铁和锌以防止腐蚀。磷酸锌骨水泥用于牙科。
虽然它在高浓度时具有腐蚀作用,但它在食品工业中被稀释用作防腐剂、酸化剂(特别是在可乐饮料中)和酸度调节剂(E 338),因为磷酸对人体无毒,除了它的腐蚀作用。也适用于制备缓冲溶液(各种“磷酸盐缓冲液”)。
生物学重要性
磷酸酯在新陈代谢中起着核心作用,尤其是作为能量和基团载体(参见例如 ATP 和 GTP)。它们是DNA、RNA、许多辅酶等的组成部分。
证明
磷酸和可溶性磷酸盐可通过与钼酸铵沉淀形成黄色磷酸钼酸铵,或在氨溶液中与镁离子沉淀形成MgNH4的方法分离。 采购订单4 证明。
来源
- ↑ RÖMPP 在线,Thieme 2007
- ↑ BGIA GESTIS 物质数据库:https://www.hvbg.de/d/bia/gestis/stoffdb/index.html . 3 月 3 日2007
- ↑ ESIS-欧洲化学物质信息系统
- 磷的其他含氧化合物