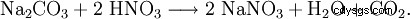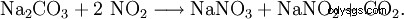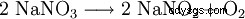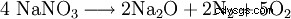| 结构式 | |||||||
|---|---|---|---|---|---|---|---|
| 好吧 | |||||||
| 常规 | |||||||
| 名字 | 硝酸钠 | ||||||
| 其他名称 |
| ||||||
| 分子式 | NaNO3 | ||||||
| CAS号 | 7631-99-4 | ||||||
| 简短说明 | 无色结晶固体 | ||||||
| 属性 | |||||||
| 摩尔质量 | 84.99 克摩尔 | ||||||
| 物质状态 | 固定 | ||||||
| 密度 | 2.26 克厘米 | ||||||
| 熔点 | 306.8 °C | ||||||
| 沸点 | 从 380 °C 开始分解 | ||||||
| 蒸气压 | <0.001hPa (25°C) | ||||||
| 溶解度 | 易溶于水:874 g/l (at 20 °C) | ||||||
| 安全说明 | |||||||
| |||||||
| MAK | 未指定 | ||||||
| LD50 | 1267 mg kg(大鼠,口服) | ||||||
| 在可能和常见的情况下,使用 SI 单位。除非另有说明,否则给出的数据适用于标准条件。 | |||||||
硝酸钠 (还有 硝酸钠 或 智利硝石 ) 是一种化合物,即硝酸的钠盐。纯态时为吸湿性(吸水性)白色物质或无色晶体。
出现次数
硝酸钠是最重要的天然硝酸盐。主要产地是智利,因此俗称智利硝石。在埃及、小亚细亚、哥伦比亚和加利福尼亚还有其他天然矿床。
提取
通过过滤通过热水浸出获得的热盐水来清除天然沉积物中的异物。在寒冷中结晶出来的硝酸钠的纯度约为 98%。母液中的碘酸盐用于碘提取。
碳酸钠与硝酸反应也可制得硝酸钠:
氨在浓碳酸钠溶液中氧化产生的残余气体的吸收在这里是理想的:
为了氧化亚硝酸盐,它用硝酸酸化,在空气中氧化成硝酸盐并用碳酸钠中和。在真空蒸发器中浓缩成固体。
属性
物理性质
- 重要的热力学性质
- Δf Hs :15.5 in kJ/mol
- Ss :116 in J/(mol K)
化学性质
在热硫酸中转化为硫酸氢钠生成硝酸:
在高于 380 °C 的温度下会分解为亚硝酸钠:
在800℃以上的温度下对氧化钠:
用法
- 肥料
- 建材行业:水泥添加剂
- 化学制造:硝酸钾
- 以前也用于生产硝酸
- 作为防腐剂 E 251
- 用于腌制肉类和香肠产品(也与亚硝酸钠 E 250 和亚硝酸钾 E 249 一起使用)
- 用于蓄热的 PCM
食品添加剂
硝酸盐可以对抗细菌,尤其是对抗可怕的肉毒杆菌(肉毒杆菌)。在固化过程中,化学上不太稳定的肌肉色素(肌红蛋白)转化为更稳定的变体(变红)。结果,肉保持其红色。未腌制的肉类和香肠会变成灰色,这被大多数消费者误认为是变质的迹象。此外,在腌制过程中会形成典型的香气。
硝酸钠用于制作香肠、硬奶酪、半硬奶酪、腌鲱鱼和鲱鱼。
硝酸盐本身是无害的。它们的使用是有问题的,因为它们会转化为亚硝酸盐。这种转化在食物中是可能的,在人体中也是可能的。亚硝酸盐具有扩张血管和降低血压的作用。在较高剂量下,它们会导致急性中毒症状。 (缺乏血色素血红蛋白=蓝瘾)。亚硝酸盐在人体内可转化为高度致癌的亚硝胺,同时吸收蛋白质。
证明
- 检测反应
- 钠:在蓝色本生灯火焰中呈亮黄色
- 硝酸盐:将物质的刮刀尖端溶解在稀硫酸中,然后加入冷的饱和硫酸铁 (II) 溶液。底层用少许浓硫酸。在边界层形成一个棕色环,这是硝酸盐的证据(环测试)。
来源
- ↑ BGIA GESTIS 物质数据库:https://www.hvbg.de/d/bia/gestis/stoffdb/index.html . 2007 年 6 月 15 日